7月9日,CDE官網(wǎng)顯示,信諾維醫(yī)藥的注射用亞胺培南西司他丁鈉福諾巴坦(簡稱注射用亞胺西福)上市申請獲正式受理。這款全球首創(chuàng)的抗菌新藥擬用于治療醫(yī)院獲得性細(xì)菌性肺炎和呼吸機相關(guān)性細(xì)菌性肺炎(HABP/VABP),直擊當(dāng)前臨床最棘手的耐藥菌感染難題。
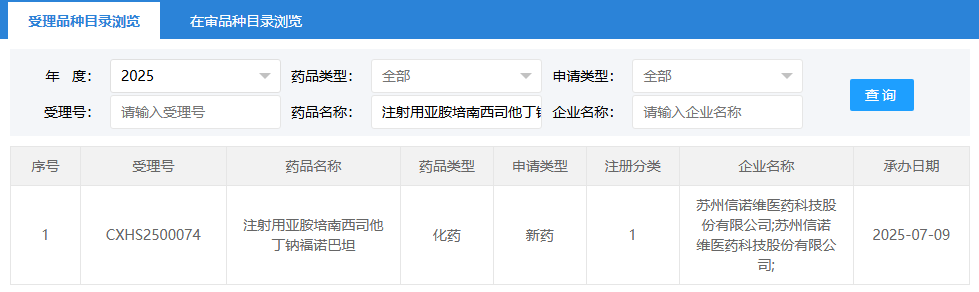
圖片來源:CDE官網(wǎng)
與其他新型β-內(nèi)酰胺酶抑制劑(如阿維巴坦、瑞萊巴坦等)相比,該產(chǎn)品具有更廣、更強的抑酶活性,能全面有效抑制革蘭陰性菌常見的A、C、D類酶活性。
這一突破性進(jìn)展背后,是一家成立僅8年的中國藥企在耐藥菌戰(zhàn)場上的關(guān)鍵突圍。
在重癥監(jiān)護病房里,醫(yī)院獲得性肺炎和呼吸機相關(guān)肺炎是危及生命的常見感染。而更令人擔(dān)憂的是,碳青霉烯類耐藥革蘭陰性桿菌的檢出率持續(xù)走高,使得傳統(tǒng)“最后一道防線”抗生素逐漸失效。
世界衛(wèi)生組織(WHO)早已將對碳青霉烯耐藥的鮑曼不動桿菌(CRAB)、銅綠假單胞菌(CRPA)和腸桿菌(CRE)列為三大具有嚴(yán)重威脅的耐藥菌。 這些耐藥菌導(dǎo)致的感染死亡率極高,臨床治療選擇極為有限。
信諾維此次申報上市的亞胺西福,正是瞄準(zhǔn)這一重大未滿足臨床需求。作為一款新型β-內(nèi)酰胺類/β-內(nèi)酰胺酶抑制劑復(fù)方制劑,它能同時有效對抗三大碳青霉烯耐藥革蘭陰性桿菌,成為全球首款具有如此廣譜抗菌活性的BL/BLI藥物。
此次申報基于XNW4107-302國際多中心III期臨床研究(Reitab Study)的積極結(jié)果。這項前瞻性、雙盲、隨機、陽性藥物對照的關(guān)鍵研究,覆蓋全球多個研究中心,共入組449例患者。
研究結(jié)果顯示,在主要終點——第14天全因死亡率方面,亞胺西福達(dá)到了非劣效性結(jié)果。更為重要的是,在臨床治療成功率和耐藥菌微生物清除率方面,該藥物表現(xiàn)出比對照組更優(yōu)異的結(jié)果。

圖片來源:藥智數(shù)據(jù)企業(yè)版——全球臨床試驗
信諾維醫(yī)藥這家成立于2017年的創(chuàng)新藥企,近年來在行業(yè)內(nèi)動作頻頻。
就在5月29日,信諾維宣布與日本安斯泰來達(dá)成一項獨家許可協(xié)議,將其靶向CLDN18.2的新一代抗體偶聯(lián)藥物XNW27011的海外權(quán)益授予安斯泰來。該交易總金額超過105億人民幣,成為今年中國創(chuàng)新藥出海的重要案例之一,根據(jù)協(xié)議,信諾維將獲得 9.35 億人民幣首付款。
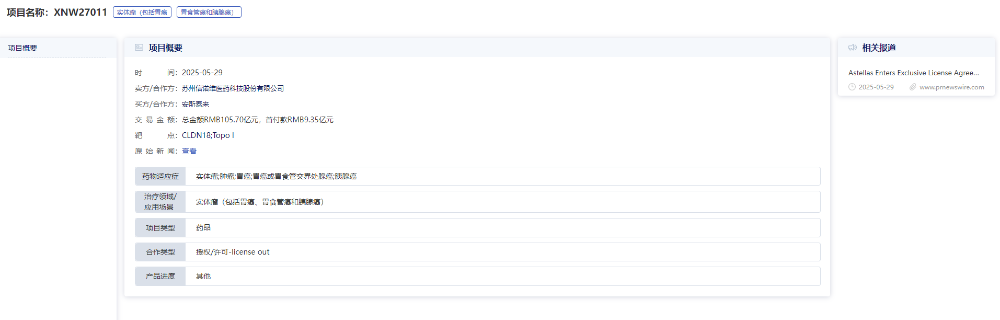
圖片來源:藥智數(shù)據(jù)企業(yè)版——投資格局
去年2月,信諾維成功完成了7億元的E輪系列融資。融資由騰訊投資和國鑫投資聯(lián)合領(lǐng)投,多家知名機構(gòu)共同參與,老股東正心谷資本持續(xù)支持。
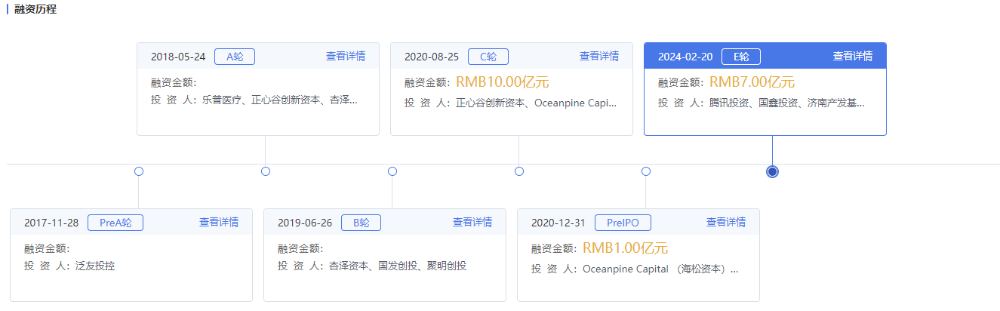
圖片來源:藥智數(shù)據(jù)企業(yè)版——投資格局
目前公司已有10個產(chǎn)品處于臨床研發(fā)階段,覆蓋腫瘤精準(zhǔn)治療、多重耐藥菌感染和代謝性疾病三大領(lǐng)域。







